Cr (хром) - элемент с прядковым номером 24 в периодической системе.
Находится в IV периоде. Температура плавления: 1857 ℃. Плотность: 7.14 г/см3.
Электронная формула
Порядок заполнения орбиталей электронами в атоме Cr является исключением из правила Клечковского.
Ожидаемая электронная формула:
1s2 2s2 2p6 3s2 3p6 4s2 3d4
Но в реальности происходит проскок одного электрона с орбитали 4s внешнего слоя на орбиталь 3d пред-внешнего слоя:
Электронная формула атома хрома в порядке возрастания энергий орбиталей:
1s2 2s2 2p6 3s2 3p6 4s1 3d5
Электронная формула атома хрома в порядке следования уровней:
1s2 2s2 2p6 3s2 3p6 3d5 4s1
Сокращенная электронная конфигурация Cr:
[Ar] 3d5 4s1
Ожидаемая электронная формула:
1s2 2s2 2p6 3s2 3p6 4s2 3d4
Но в реальности происходит проскок одного электрона с орбитали 4s внешнего слоя на орбиталь 3d пред-внешнего слоя:
Электронная формула атома хрома в порядке возрастания энергий орбиталей:
1s2 2s2 2p6 3s2 3p6 4s1 3d5
Электронная формула атома хрома в порядке следования уровней:
1s2 2s2 2p6 3s2 3p6 3d5 4s1
Сокращенная электронная конфигурация Cr:
[Ar] 3d5 4s1
Электронно-графическая схема
Ниже приведена схема распределения электронов по атомным орбиталям в атоме хрома

1-й уровень (K): 2
2-й уровень (L): 8
3-й уровень (M): 13
4-й уровень (N): 1
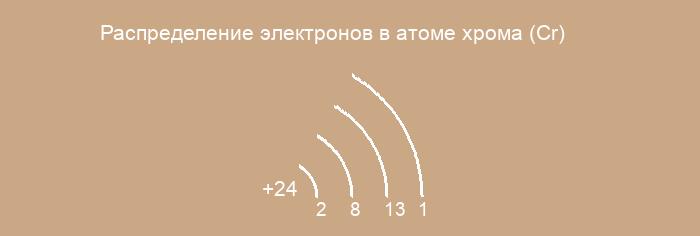

Энергетические уровни
Распределение электронов по энергетическим уровням в атоме Cr1-й уровень (K): 2
2-й уровень (L): 8
3-й уровень (M): 13
4-й уровень (N): 1

Валентные электроны хрома
Количество валентных электронов в атоме хрома - 6.
Ниже приведены их квантовые числа (N - главное, L - орбитальное, M - магнитное, S - спин)
Ниже приведены их квантовые числа (N - главное, L - орбитальное, M - магнитное, S - спин)
| Орбиталь | N | L | M | S |
|---|---|---|---|---|
| s | 4 | 0 | 0 | +1/2 |
| d | 3 | 2 | -2 | +1/2 |
| d | 3 | 2 | -1 | +1/2 |
| d | 3 | 2 | 0 | +1/2 |
| d | 3 | 2 | 1 | +1/2 |
| d | 3 | 2 | 2 | +1/2 |
Степени окисления, которые может проявлять хром: +1, +2, +3, +4, +5, +6
Стабильные изотопы
| Изотоп | Кол-во протонов | Кол-во нейтронов | Атомная масса изотопа |
|---|---|---|---|
| 50Cr | 24 | 26 | 49.9460442 |
| 52Cr | 24 | 28 | 51.9405075 |
| 53Cr | 24 | 29 | 52.9406494 |
| 54Cr | 24 | 30 | 53.9388804 |
Другие элементы
Электронные формулы других элементов
Электронная формула ванадия (V)Электронная формула марганца (Mn)
Таблица электронных конфигураций
